Ličio amidasyra cheminė medžiaga, kurios cheminė formulė yra LiNH2 ir CAS 7782-89-0. Tai balti, blizgūs kristaliniai milteliai su amoniako kvapu, netirpūs žibale, tirpūs skystame amoniake, tirpsta šaltame vandenyje ir stipriai hidrolizuojasi veikiant karštam vandeniui. Lydymosi temperatūra 380-400 laipsnių, virimo temperatūra 430 laipsnių, santykinis tankis 1,17817,5. Ištirpinti šaltame vandenyje, suskaidyti į ličio hidroksidą ir amoniaką karštame vandenyje, ištirpinti druskos rūgštyje, kad susidarytų ličio chloridas ir amonio chloridas, šiek tiek tirpus skystame amoniake ir etanolyje, netirpus eteryje ir benzene. Lėtai suyra ore, bet nedega. Kaitinamas iki 450 laipsnių vakuume, jis suyra į LiNH3 ir NH3. Tai stipri bazė, kuri lengvai reaguoja su siera ir selenu. Lengvai oksiduojamas, gali būti oksiduojamas azoto dioksidu iki ličio azido. Reaguoja su koncentruota druskos rūgštimi, kad susidarytų laisvas amoniakas. Turi nedidelį korozinį poveikį stiklui. Daugiausia naudojama organinėje sintezėje ir vaistų gamyboje, tai yra gera vandenilio saugojimo medžiaga kartu su ličio hidridu ir ličio iminu.

|
|
|
|
Cheminė formulė |
H2LiN |
|
Tikslios Mišios |
23 |
|
Molekulinė masė |
23 |
|
m/z |
23 (100.0%), 22 (8.2%) |
|
Elementų analizė |
H 8,78; Li, 30,22; N 61,00 |

Ličio amidasgali būti naudojamas nitrilų ir ketonų alkilinimui, acetileno junginių sintezei ir kt. Taikymo pavyzdžiai yra tokie:
1. Chiralinio sulfonamido sintezė.
Chiraliniai alkilo (aril) sulfonilamidai turi svarbią taikymo reikšmę smulkiojoje organinėje sintezėje ir chiralinėje vaistų sintezėje. Naudojant jį kaip chiralinį kofaktorių, daugelis chiralinių aminų junginių ir chiralinių vaistų, kuriuos sunku susintetinti įprastais būdais, gali būti asimetriškai susintetinti. Techninis sprendimas yra: chiralinio sulfonamido sintezės metodas, naudojant chiralinį tiosulfonamidą kaip žaliavą ir redukuojant jį skystu amoniaku amino ličio, kad būtų gautas chiralinis sulfonamidas. Reakcijos formulė yra tokia:

Tarp jų R yra vienas iš šių: C1-C10 alkilas, fenilas, paratoluenas, ortometilfenilas, metametilfenilas, paraetilfenilas, para-tret-butilfenilas, paraacetilfenilas, ortoacetilfenilas, naftilas. Veiksmai yra tokie:
1 veiksmas:
Paruoškite LiNH2, naudodami ličio metalą ir skystą amoniaką;
2 veiksmas:
Į chiralinį tiosulfinato tirpalą įlašinkite LiNH2, po to, kai lašinamas įpylimas, maišykite reakciją ir tęskite 2-20 valandų, kai reakcijos temperatūra yra -80 laipsnių -80 laipsnių;
3 veiksmas:
Reakcijai pasibaigus, į sistemą įpilkite ledo kubelių ir ekstrahuokite dichlormetanu. Sumaišykite organines fazes ir pašalinkite tirpiklį, kad gautumėte rausvai rudą kietą medžiagą. Perkristalizuokite iš n-heksano, kad gautumėte didelės ee vertės chiralinį sulfonamidą.
2. Aktyvi ličio talpykla ličio -jonų akumuliatoriams.
Jis naudojamas negrįžtamiems pradiniams nuostoliams sumažinti ir yra universalus ličio šaltinis elektrodų medžiagoms ir ličio akumuliatoriams arba kaip universalus ličio šaltinis, kai miltelių pavidalo ličio tiekimo medžiaga, kurios elektrocheminis potencialas, palyginti su Li/Li+, yra 0,5-2V, yra naudojama kaip aktyvi ličio saugykla, pasirinkta iš ličio hidrido, tetraamino ličio, imino ličio ir amonio. Šie junginiai suyra ir išskiria ličio bei dujinius šalutinius produktus, kai viršija standartinį oksidacijos potencialą savo elektrocheminėje kameroje, panaudojus atitinkamą potencialą.
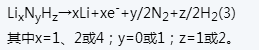

Ličio amidas (LiNH2), kaip svarbi cheminė medžiaga, plačiai naudojamas įvairiose srityse.

Organinė sintezė
LiNH2 vaidina lemiamą vaidmenį organinės sintezės srityje. Tai ne tik įvairių organinių reakcijų katalizatorius ir reagentas, bet ir skatina sudėtingų organinių junginių sintezę.
1. Katalizatoriai ir reagentai
Bendrovė atliko konkurencinio pranašumo analizę, kad nustatytų savo stipriąsias ir silpnąsias puses, palyginti su konkurentais.
(1) Kondensacijos skatintojas:
LiNH2 pasižymi puikiomis katalizinėmis savybėmis aldolio kondensacijos reakcijose ir kitose kondensacijos reakcijose, skatindamas veiksmingą reagentų jungimąsi.
(2) Reduktorius:
Organinėje sintezėje LiNH2 dažniausiai naudojamas kaip reduktorius, dalyvaujantis įvairiose redokso reakcijose ir padedantis sintezuoti tikslinius junginius.


(3) Sausinimo medžiaga ir sausiklis:
Tais atvejais, kai iš reakcijos sistemos reikia pašalinti vandenį, LiNH2 gali veikti kaip sausinantis agentas ir sausiklis, užtikrinantis sklandų reakcijos eigą.
(4) Dehalogeninimo ir alkilinimo agentai:
LiNH2 taip pat yra nepakeičiamas katalizatorius ir reagentas halogenintų angliavandenilių dehalogeninimo ir alkilinimo reakcijose.
(5) Aminolizės reagentas:
Amonolizės reakcijoje LiNH2 gali skatinti reagentų ir amoniako reakciją, sudarydamas atitinkamus amonolizės produktus.
2. Polimerizacijos iniciatorius
LiNH2 taip pat gali būti naudojamas kaip etileno junginių anijoninės polimerizacijos iniciatorius, skatinantis polimerizacijos reakciją ir taip sintetinant polimerinius junginius.
3. Specifinių junginių sintezė
LiNH2 gali būti naudojamas gaminant specifinius junginius, tokius kaip azidai ir cianidai, toliau plečiant jo taikymo sritį organinėje sintezėje.


Vaistų gamyba
Farmacijos pramonėje LiNH2 taip pat vaidina svarbų vaidmenį. Tai svarbus katalizatorius ir žaliava įvairių vaistų sintezei.
1. Vitaminų sintezė
LiNH2 yra svarbus junginių, tokių kaip vitaminas A ir vitaminas D3, sintezės katalizatorius. Dėl katalizinio poveikio šie žmogaus sveikatai būtini vitaminai gali būti efektyviai sintezuojami.
2. Vaistų sintezės katalizatorius
Gaminant antioksidantus 1010 ir 1076, LiNH2 taip pat naudojamas kaip efektyvus nitrilų ir ketonų alkilinimo reakcijos katalizatorius. Šie antioksidantai atlieka svarbų vaidmenį vaistų sintezėje ir konservavime.
Vandenilio saugojimo medžiaga
Nors pats LiNH2 negrįžtamai išskiria NH3 kaitinant, todėl jis netinkamas tiesiogiai naudoti kaip vandenilio kaupimo medžiaga, derinant su LiH ar kitomis vandenilio laikymo medžiagomis, jis gali veiksmingai slopinti amoniako išsiskyrimą ir yra gerai grįžtamas. Todėl sudėtinių vandenilio saugojimo medžiagų srityje LiNH2 turi svarbų pritaikymo potencialą.


Laboratorinis naudojimas
Laboratorijoje LiNH2 taip pat dažnai naudojamas kitiems junginiams ruošti arba specifiniams cheminių reakcijų tyrimams atlikti. Dėl savo unikalių cheminių savybių ir plačių pritaikymo galimybių LiNH2 tapo vienu iš nepakeičiamų reagentų chemijos laboratorijose.

1) Kaitinant ličio metalą amoniako dujose, galima gauti didesnį kiekįLičio amidas. Ličio metalas dedamas į ploną nikelio griovelį, kuris vėliau dedamas į stiklinį vamzdelį. Vamzdis pakreipiamas elektrinėje krosnyje ir įkaitinamas iki 380-400 laipsnių. Amoniako dujos įleidžiamos iš vieno vamzdžio galo, o išlydytas LiNH2 išteka iš kito galo ir sukietėja reakcijos vamzdžio aušinimo skyriuje. Tokiu būdu ličio metalas gali nuolat atskleisti savo šviežią paviršių ir užtikrinti nuolatinę reakciją.
2) Sudėkite du nikelio tiglius vieną ant kito ir įdėkite juos į vertikalų stiklinį vamzdelį. Išgręžkite tris 15 mm mažas skylutes viršuje esančio nikelio tiglio apačioje. Kaitinamas iki 400 laipsnių amoniako sraute, išlydytas LiNH2 gali nuolat lašėti į žemiau esantį tiglį ir atvėsti bei kietėti amoniako sraute. LiNH2 yra bespalvė, skaidri ir blizgi kristalinė medžiaga. Santykinis tankis 1,178 (17,5 laipsnio). Lydymosi temperatūra 380-400 laipsnių. Kaitinamas iki 450 laipsnių vakuume, jis gali suskaidyti ir išskirti amoniako dujas bei generuoti ličio imną. Li2NH 750-800 laipsnių temperatūroje skyla į LiNH2.

Charlesas Hauseris pirmą kartą panaudojo LiNH2 kaip bazę šeštajame ir šeštajame dešimtmečiuose. Skystame amoniake esantis aminoličio kiekis gali būti naudojamas TBA enolio ličiui gaminti, taip pat įvairiose ketonų ir aldehido substratų aldolio kondensacijos reakcijose. J In Org. Chem. 1960, 25, 503-507, Hauseris išplėtė savo pradinį darbą, įtraukdamas ličio enolio reakciją su įvairiais ketonų ir aldehidų substratais, įskaitant etilo acetatą. Yra tyrimų, kuriuose LiNH2 naudojamas kaip kryžminės Claiseno kondensacijos reakcijos tarp struktūrų, apimančių tret. butilacetato enolatą, ir struktūrų, apimančių ECHB ir HN, pagrindas, kuris yra ilgo sąrašo, kuriame yra daugiau trukdomų bazių, dalis. Aprašytas metodas yra metodas, kurio reakcijos laikas yra trumpesnis nei 5 minutės. Tačiau buvo nustatyta, kad vien LiNH2 negali būti veiksmingai naudojamas kaip bazė reakcijose, aprašytose šioje esamoje techninėje literatūroje, galbūt dėl mažo tirpumo.
Taip pat yra tyrimų naudojantLičio amidasskystame amoniake Claiseno esterių savaiminio kondensacijos reakcijai. Tačiau skystame amoniake esantis aminolitis laikomas netinkamu kryžminėms Claisen kondensacijos reakcijoms, ypač Claiseno kondensacijos reakcijoms, kai viename ar keliuose esteriuose yra hidroksilo grupių. Manoma, kad skystame amoniake esantis aminoličio kiekis iš pradžių deprotonuoja alkoholio grupę ir susidaro alkoholio litis. Šios alkoholio druskos ličio metalas yra idealioje padėtyje, kad galėtų koordinuotis su gretimomis esterių grupėmis, ir šis koordinavimas padidina esterio reaktyvumą nukleofilinio pakeitimo atžvilgiu.
Koks yra šio junginio šalutinis poveikis?
Šio junginio šalutinis poveikis daugiausia susijęs su galimu pavojumi žmonių sveikatai ir aplinkai. Toliau pateikiama išsami jo šalutinio poveikio analizė:
1.Šalutinis poveikis žmonių sveikatai
Ūmus toksiškumas
Kontaktas su oda:
Jis stipriai dirgina ir ėsdina odą. Po sąlyčio su oda gali atsirasti tokių simptomų kaip paraudimas, patinimas, skausmas ir nudegimai. Sunkiais atvejais tai gali sukelti odos nekrozę arba nuolatinius randus.
Akių kontaktas:
Ši medžiaga taip pat stipriai dirgina akis ir gali sukelti akių skausmą, ašarojimą, paraudimą ir net ragenos pažeidimą ar aklumą.
Ūmus toksiškumas
Įkvėpimas:
Įkvėpus šios medžiagos garų ar dulkių, gali sudirginti kvėpavimo takus ir atsirasti tokių simptomų kaip kosulys, švokštimas ir pasunkėjęs kvėpavimas. Sunkiais atvejais tai gali sukelti kvėpavimo takų ligas, tokias kaip cheminė pneumonija ir plaučių edema.
Nurijimas:
Atsitiktinai nurijus, gali atsirasti virškinimo trakto erozija, dėl kurios gali atsirasti tokių simptomų kaip pykinimas, vėmimas, pilvo skausmas ir viduriavimas. Sunkiais atvejais tai gali kelti pavojų gyvybei.
Ilgalaikio{0}} poveikio poveikis
Ilgalaikis šio junginio poveikis gali sukelti lėtinį apsinuodijimą ir pakenkti kelioms žmogaus kūno sistemoms. Tai apima nervų sistemą, kvėpavimo sistemą, virškinimo sistemą, reprodukcinę sistemą ir tt Konkretūs simptomai gali skirtis priklausomai nuo individualių skirtumų, bet paprastai apima galvos skausmą, galvos svaigimą, atminties praradimą, koncentracijos stoką, kvėpavimo pasunkėjimą, virškinimo sutrikimus, sumažėjusį vaisingumą ir kt.
2.Šalutinis poveikis aplinkai
Oro tarša
Veikiamas atviros liepsnos, didelio karščio ir gali sukelti stiprias chemines reakcijas, kai liečiasi su rūgštimis ar oksiduojančiomis medžiagomis, gali išsiskirti toksiškos dujos. Jei šios dujos bus išmestos į orą, jos užterš oro kokybę ir kels grėsmę žmonių sveikatai.
Vandens tarša
Reaguodamas su vandeniu arba vandens garais, gali išsiskirti toksiškos arba degios dujos, taip pat gali susidaryti kenksmingos nuotekos. Jei šios nuotekos bus išleidžiamos tiesiai į vandens telkinius, jos tinkamai neapdorotos, jos sukels toksiškumą vandens organizmams ir pakenks vandens ekosistemoms.
Dirvožemio tarša
Dirvožemyje esantys likučiai gali neigiamai paveikti dirvožemio mikroorganizmus ir augalus. Jis gali slopinti dirvožemio mikroorganizmų veiklą, sutrikdyti dirvožemio ekologinę pusiausvyrą, o augalams pasisavintas gali patekti į žmogaus organizmą per maisto grandinę, keldamas potencialų pavojų žmonių sveikatai.
3.Saugus naudojimas ir apsaugos priemonės
Naudojant, reikia griežtai laikytis saugos darbo procedūrų, kad būtų užtikrintas personalo ir aplinkos saugumas. Jis turi būti naudojamas gerai vėdinamoje aplinkoje, kad būtų išvengta ilgalaikio garų ar dulkių įkvėpimo. Venkite tiesioginio sąlyčio su oda ir naudokite tinkamus apsauginius drabužius, pirštines ir veido skydelius. Po naudojimo nedelsdami nusiplaukite rankas ir veidą, kad išvengtumėte odos sudirginimo dėl likučių.
Jis turi būti laikomas vėsioje, sausoje, gerai vėdinamoje vietoje, toliau nuo ugnies ir šilumos šaltinių. Sandėliavimo talpykla turi būti gerai uždaryta, kad būtų išvengta nuotėkio ir išgaravimo. Transportavimo metu reikia imtis apsaugos nuo nuotėkio priemonių, kad būtų užtikrintas saugus transportavimas. Transporto priemonėse turi būti įrengta atitinkama gaisro gesinimo- įranga ir reagavimo į avarijas įranga.
Įvykus nuotėkiui ar nelaimingam atsitikimui, reikia nedelsiant imtis skubių priemonių, pavyzdžiui, evakuoti personalą, atjungti gaisro šaltinį ir naudoti atitinkamą gaisro gesinimo įrangą. Ištekėjusią medžiagą reikia nedelsiant adsorbuoti adsorbuojančiomis medžiagomis, tokiomis kaip smėlis ir aktyvuota anglis, ir surinkti į konteinerį, kad būtų galima tinkamai pašalinti. Darbuotojai, kurie liečiasi su nutekėjusiomis medžiagomis, turi nedelsdami nusivilkti užterštus drabužius, nuplauti odą dideliu kiekiu vandens ir kuo greičiau kreiptis į gydytoją. Jei pacientas netyčia įkvėpė garų ar dulkių, jį reikia nedelsiant išnešti į gryną orą, užtikrinti, kad kvėpavimo takai būtų laisvi ir kuo greičiau kreiptis į gydytoją.
fak
Kam naudojamas ličio amidas?
Ličio amidas yra bespalvis arba pilkas kristalas arba milteliai, turintys amoniako kvapą. Jis naudojamasvaistams gaminti, chemijos gamyboje ir kaip katalizatorius.
Ar ličio amidas yra stipri bazė?
Ličio amidai yra labai reaktyvūs junginiai. Tiksliau,jie yra tvirti pagrindai.
Koks yra ličio amido tirpumas?
Ličio amido milteliai yra balti milteliai, kurių lydymosi temperatūra yra 375 laipsnių, o virimo temperatūra - 430 laipsnių. Tai yratirpsta skystame amoniakeo jo santykinis tankis yra 1,178 (17,5 laipsnio).
Ar LDA yra stipri ar silpna bazė?
Populiarus Žymos: ličio amidas cas 7782-89-0, tiekėjai, gamintojai, gamykla, didmeninė prekyba, pirkti, kaina, urmu, parduoti









